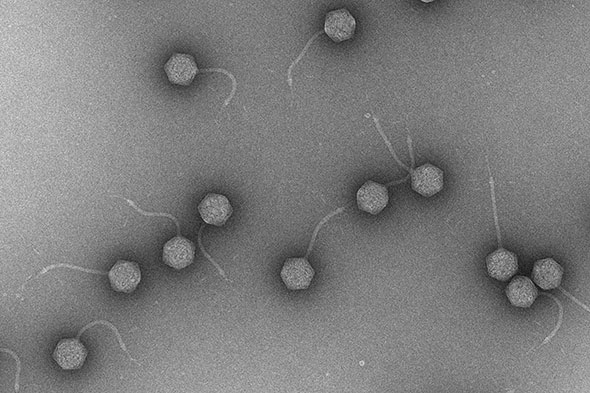
Photographie en microscopie électronique de ces virus, prédateurs naturels des bactéries. Une goutte d’eau de mer en contient plus d’un million.
© Frank Oechslin, Département de microbiologie fondamentale
Avant l’apparition des antibiotiques, on utilisait des virus pour lutter contre les bactéries pathogènes. Cet ancien traitement, aujourd’hui abandonné dans nos pays, pourrait connaître une seconde vie. La phagothérapie offre en effet une alternative aux antibiotiques qui se heurtent de plus en plus à la résistance des bactéries. Dans ce domaine, les chercheurs de l’UNIL et du CHUV font figure de pionniers, en Suisse et en Europe.
C’est devenu un véritable problème de santé publique: de plus en plus de bactéries s’adaptent aux antibiotiques censés les éliminer. En l’absence d’alternative à ces médicaments, certains experts estiment que «ces microbes résistants pourraient provoquer 10 millions de décès d’ici à 2050, soit plus que le cancer», souligne Grégory Resch, maître-assistant suppléant au Département de microbiologie fondamentale de l’UNIL.
Compte tenu de l’augmentation du phénomène de résistance, les médecins risquent d’être bientôt démunis face à de nombreuses infections devenues intraitables. D’autant que «la mise sur le marché de nouveaux antibiotiques a drastiquement chuté depuis 1980», constate Yok-Ai Que, médecin-adjoint au Service de médecine intensive adulte du CHUV.

Maître-assistant suppléant au Département de microbiologie fondamentale.
Nicole Chuard © UNIL
Des «mangeurs» de bactéries
L’une des solutions pour sortir de cette impasse pourrait venir des bactériophages, ces virus qui sont des prédateurs naturels des bactéries. Leur nom vient des termes grecs baktêria (bâton, à cause de la forme des premières bactéries observées) et phagos (mangeur).
En fait, ces phages, comme on les appelle aussi, ne «mangent» pas les micro-organismes. Comme tous les virus, ils ont besoin de la machinerie enzymatique d’une cellule hôte pour se multiplier. A cette fin, ils utilisent donc une bactérie qu’ils détruisent une fois leur réplication achevée.
Ces bactériophages ont véritablement colonisé la planète. «Ils sont présents là où il y a des bactéries», souligne Grégory Resch et l’on estime qu’il y aurait sur terre 1031 particules (dix mille milliards de milliards de milliards !), ce qui fait d’eux «l’entité biologique la plus représentée à la surface du globe». Ils affectionnent tout particulièrement le sol et les eaux usées, mais on en trouve partout, y compris dans les eaux de surface «où il y en a plus de 1 million par goutte d’eau de mer, précise le microbiologiste. Quand vous vous baignez et que vous buvez la tasse, vous en ingurgitez des milliards !» Le corps humain (les intestins, la salive, le nez, etc.) en renferme aussi.
Le pouvoir bactéricide des eaux du Gange
Fort heureusement, ces virus sont inoffensifs pour l’être humain. Non seulement ils ne s’attaquent qu’aux bactéries, mais en outre chacun d’eux ne s’en prend qu’à une proie particulière – «un phage qui détruit une Escherichia coli ne va pas s’attaquer à un streptocoque», précise Grégory Resch – et même à un nombre limité de souches de cette espèce. Cette spécificité fait d’eux des alliés de choix dans la lutte contre les maladies infectieuses d’origine bactérienne.
La découverte de l’activité bactéricide des phages remonte aux années 1890. Parti en Inde pour analyser les eaux du Gange, le bactériologiste britannique Ernest Hankin «a été surpris de n’y trouver que très peu de vibrions du choléra, alors que cette maladie provoquait des épidémies dans le pays, raconte le microbiologiste de l’UNIL. C’était d’autant plus étonnant qu’à l’époque, on pensait que les bactéries étaient véhiculées par les fleuves.» C’est ainsi que le chercheur britannique a compris que ces eaux contenaient des particules qui avaient un pouvoir antibactérien. «Il n’a pas deviné qu’il s’agissait de virus, mais il a mis le phénomène en évidence pour la première fois.»
Il a ensuite fallu attendre 1917 pour qu’un chercheur franco-canadien travaillant à l’Institut Pasteur, Félix d’Hérelle, isole ces agents actifs – auxquels il a donné leur nom de bactériophages – dans les selles de patients infectés. «Il a constaté qu’en introduisant d’importantes quantités de phages dans les puits de villages en Inde, on parvenait à éradiquer une épidémie de choléra en deux jours au lieu de sept», selon Grégory Resch. Malgré le scepticisme de nombre de ses collègues, Félix d’Hérelle a proposé d’utiliser ces virus en médecine humaine et, à partir de 1919, ils ont été employés pour traiter les infections bactériennes.
L’âge d’or des bactériophages s’est terminé dix ans plus tard avec l’arrivée sur le marché des premiers antibiotiques. On disposait alors de médicaments «qui sont faciles à utiliser, qui donnent de bons résultats et dont le modèle économique a beaucoup de succès: l’industrie les produit, les médecins les prescrivent et les patients les reçoivent», explique Yok-Ai Que. Grâce à eux, on pensait pouvoir éradiquer les épidémies. Les phages sont donc tombés en désuétude. Ce qui n’a pas empêché un chercheur lausannois, Jean-Pierre Feihl, de faire, en 1949, sa thèse sur «La thérapeutique des staphylococcies par le bactériophage», dans laquelle il expliquait qu’il avait guéri 83% des 77 patients qu’il avait traités avec des phages.
Mais il en aurait fallu beaucoup plus pour faire de l’ombre aux antibiotiques qui avaient fait leurs preuves et relégué les virus tueurs de bactéries au rang d’antiquités. La phagothérapie a depuis été totalement abandonnée en Europe de l’Ouest, et notamment en Suisse. Elle est cependant toujours utilisée en Russie, en Pologne et en Géorgie, pays qui abrite un institut dédié à la recherche et à l’application médicale des bactériophages, le George Eliava Institute of Bacteriophages, Microbiology and Virology, ainsi qu’un centre consacré à la thérapie. «Les médecins y traitent chaque année 2000 patients, atteints surtout d’infections urinaires et intestinales, uniquement avec des bactériophages», constate Grégory Resch, qui a passé récemment plusieurs semaines en Géorgie.
Dans le reste de l’Europe, la roue est toutefois en train de tourner pour les phages, car les antibiotiques ont montré leurs limites. De plus en plus de bactéries se sont en effet adaptées à ces médicaments auxquelles elles opposent de la résistance. Pour faire face à ce phénomène inquiétant, les chercheurs et médecins s’intéressent donc à nouveau à la phagothérapie. «Leur spécificité était auparavant le talon d’Achille de ces virus, car il était beaucoup plus aisé d’utiliser des antibiotiques à large spectre. Aujourd’hui, cela devient l’un de leurs principaux avantages», explique Yok-Ai Que. La phagothérapie nécessite toutefois «un couplage entre le diagnostic microbiologique et la prescription des phages», ajoute le médecin intensiviste. Fort heureusement, on dispose actuellement de techniques capables d’identifier rapidement l’agent pathogène afin de savoir quel virus utiliser. Il est aussi possible d’utiliser des cocktails de bactériophages, ce qui élargit leur spectre d’action.

Médecin-adjoint au Service de médecine intensive adulte
du CHUV. Nicole Chuard © UNIL
Les phages ne détruisent pas la flore intestinale
Autre intérêt de ces virus: ils ne s’attaquent pas aux bactéries commensales (qui vivent à l’intérieur de notre organisme). D’ailleurs, nos intestins en renferment une grande quantité. Contrairement aux antibiotiques, souligne Grégory Resch, «ils ne détruisent donc pas la flore intestinale», le fameux microbiote dont on mesure aujourd’hui l’importance pour notre santé. En outre, «en nonante ans d’expériences, les Géorgiens disent n’avoir jamais constaté de complications graves, poursuit le microbiologiste. Au pire, ils n’ont observé que quelques poussées de fièvre chez leurs patients.»
Certes, comme avec les antibiotiques, on pourrait aussi observer avec les phages des phénomènes de résistance, mais ceux-ci devraient pouvoir être plus facilement maîtrisés. «Contrairement aux médicaments, les phages ont co-évolué avec leurs hôtes depuis des millions d’années, constate Yok-Ai Que. Dans la nature, si une bactérie devient résistante à un phage, elle se multiplie et la probabilité qu’elle rencontre un autre virus auquel elle est sensible augmente. Aussitôt, celui-ci se reproduit en grandes quantités et il parvient à contrôler l’expansion de la bactérie.» En cas de résistance, «le répertoire de phages disponibles dans la nature étant presque infini, on trouvera sans doute plus aisément la parade en recherchant d’autres phages, ajoute Grégory Resch. Leur identification et leur isolation ne prennent que quelques jours, alors qu’il faut des années de recherche pour mettre au point un nouvel antibiotique potentiel.»
Dans les eaux usées des stations d’épuration
En outre, les phages ne sont pas particulièrement difficiles à cultiver. «Dans notre laboratoire, précise Grégory Resch, nous isolons les bactériophages à partir d’échantillons d’eaux usées que nous récupérons notamment à la station d’épuration de Vidy. Une fois centrifugés (pour éliminer les bactéries restantes), puis filtrés, ces échantillons donnent une “soupe” renfermant de nombreux phages que l’on isole en les mettant en contact avec la bactérie qui nous intéresse.» Ils se reproduisent alors très rapidement. Les bactériophages ainsi obtenus peuvent ensuite être conservés pendant plusieurs années à 4 °C; ils peuvent aussi être congelés ou lyophilisés.
Ça marche, mais il faudra quand même le prouver !
Les bactériophages présentent donc de nombreux avantages. Pourquoi tarder à les utiliser dans la pratique clinique, comme on le faisait au début du XXe siècle ? «La documentation scientifique existante n’a pas la qualité requise aujourd’hui par les agences de régulation des médicaments, comme Swissmedic en Suisse», répond Yok-Ai Que. Pour que les phages puissent recevoir une autorisation de mise sur le marché, il faut que leur fabrication réponde aux critères très stricts de “bonne pratique de fabrication” et de “bonne pratique des essais cliniques”. Autant dire que les chercheurs et médecins doivent remettre l’ouvrage sur le métier et – presque – tout reprendre à zéro, comme cela se fait pour n’importe quel médicament, afin de prouver scientifiquement l’intérêt et l’innocuité de la phagothérapie.
C’est à cette tâche que Yok-Ai Que, Grégory Resch et leurs collègues de l’UNIL et du CHUV se sont attelés. Ils participent à la première étude clinique européenne sur la phagothérapie, Phagoburn (lire l’article). Par ailleurs, dans le cadre du programme SCOPES du FNS (qui favorise les échanges scientifiques entre le Suisse et les pays d’Europe de l’Est), ils collaborent avec leurs collègues de l’Institut géorgien. «Nous étudions des bactériophages qui luttent contre les Acinetobacter. Les Géorgiens isolent des phages que, dans notre laboratoire, nous séquençons et testerons sur un modèle animal. Notre objectif est de trouver un cocktail de phages actifs contre cette bactérie résistante aux antibiotiques.»
Autre projet: la constitution d’une banque de phages. Pour traiter rapidement les patients infectés par une bactérie pathogène, les médecins doivent en effet pouvoir disposer très rapidement des phages adéquats. «Grâce à une subvention que nous avons reçue de la Loterie Romande, nous allons isoler, identifier et séquencer 150 phages cette année et autant l’année prochaine», précise Yok-Ai Que.
Les projets ne manquent donc pas. L’UNIL et le CHUV comptent ainsi conforter leur rôle de pionniers en remettant au goût du jour la phagothérapie qui fournira aux médecins une nouvelle arme, complémentaire aux antibiotiques, pour lutter contre les bactéries pathogènes.
Phageback, un atelier ouvert au public
Le laboratoire public de l’UNIL, L’Eprouvette, propose à tout un chacun de se familiariser avec les phages. Dans le cadre du programme Agora du FNS qui vise à favoriser la communication entre les chercheurs et le public, un atelier bactériophage, «Phageback, le retour des virus guérisseurs», a été ouvert en février 2015. «Les visiteurs vont récupérer un échantillon d’eau usée à la station d’épuration de Vidy, comme nous le faisons dans notre laboratoire, explique Grégory Resch, chercheur au Département de microbiologie fondamentale de l’UNIL. Puis ils reviennent à L’Eprouvette pour isoler les phages qu’ils peuvent ensuite observer à la plate-forme de microscopie électronique et photographier.» Outre cet atelier, des expositions et des débats seront aussi organisés afin «de discuter avec le public des enjeux de la phagothérapie», conclut le microbiologiste.
Inscriptions et renseignements: mathilde.ythier@unil.ch
Article suivant: Phagothérapie: premier essai clinique au CHUV



