Cette étude explore comment la combinaison de l’intelligence artificielle (IA) avec des caractéristiques traditionnelles des images de l’œil améliore la prédiction des maladies et la découverte de gènes associés. En analysant des images rétiniennes à l’aide du modèle d’apprentissage profond RETFound et en comparant ses résultats à des traits mesurables connus des médecins, les chercheurs montrent que l’intégration des deux approches permet des prédictions de santé plus précises et une meilleure compréhension biologique.
Combiner l’IA et les traits traditionnels des images de l’œil améliore la détection des maladies et des gènes
L’intelligence artificielle (IA) permet aux médecins d’analyser plus efficacement les images médicales et de prédire les risques de maladies. Une approche puissante, appelée « apprentissage profond » (deep learning), est capable d’identifier des motifs complexes dans les images de la rétine. Cependant, ces systèmes produisent souvent des résultats difficiles à interpréter, ce qui complique leur adoption par les professionnels de santé.
Dans une étude récente, un groupe de chercheurs a analysé un modèle d’apprentissage profond nommé RETFound, entraîné à partir de millions d’images oculaires. Les performances de ce modèle ont été comparées à celles de caractéristiques visuelles plus classiques, comme la forme ou la taille des vaisseaux sanguins — des traits déjà bien connus et utilisés en ophtalmologie.
Les résultats ont montré que les motifs internes appris par RETFound ne correspondaient pas directement aux traits traditionnels pris individuellement. En revanche, la combinaison des deux approches permettait de meilleures performances. Les chercheurs ont également entraîné RETFound à prédire ces traits classiques : bien que les prédictions soient proches des valeurs mesurées, elles restent imparfaites.
Par ailleurs, les caractéristiques apprises par RETFound se sont révélées associées à de nombreux gènes, souvent différents de ceux liés aux traits traditionnels. Certaines de ces caractéristiques présentaient une influence génétique plus marquée et s’avéraient plus efficaces pour prédire certaines maladies oculaires.
Concernant des problèmes de santé plus généraux — comme le diabète, la tension artérielle ou le poids corporel —, les caractéristiques issues de l’IA ont montré une grande utilité. Mais c’est bien la combinaison des traits IA et traditionnels qui a donné les prédictions les plus précises.
En résumé, cette étude démontre que l’association de traits visuels compréhensibles par l’humain avec des caractéristiques apprises par l’IA permet une meilleure évaluation de la santé oculaire et des maladies associées, ouvrant la voie à des diagnostics plus fiables et à une compréhension approfondie des mécanismes pathologiques.
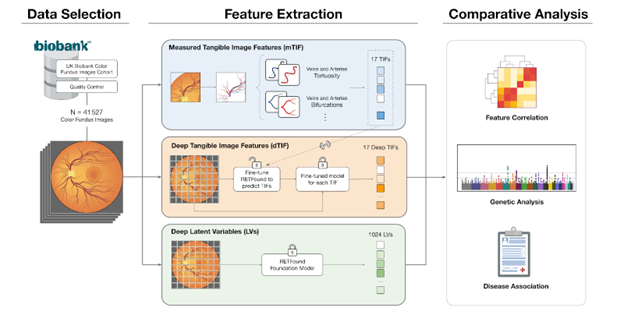
(c) Pour les analyses comparatives ultérieures, des corrélations directes, des associations génétiques et des liens avec diverses maladies ont été étudiés.
Preprint: https://doi.org/10.1101/2024.12.23.24319548
Sven Bergman dirige actuellement le projet Sinergia financé par le FNS, intitulé « Connecter les propriétés de la micro- et macrovascularisation à partir d’imagerie multimodale grâce à la génétique et à l’apprentissage profond, afin de mieux comprendre les mécanismes pathologiques vasculaires et de prédire les risques de maladies », en collaboration avec trois partenaires médicaux : l’Hôpital ophtalmique Jules-Gonin, l’Inselspital de Berne et l’Erasmus Medical Center de Rotterdam.
L’objectif de ce projet est de mieux comprendre l’interaction entre différents types de vaisseaux sanguins, à différentes échelles et dans divers organes, allant des très petites capillaires aux grandes artères et veines. En utilisant de vastes collections d’images médicales, le projet vise à mesurer les propriétés des vaisseaux, à les relier entre elles, et à étudier leur contribution au risque de maladies cardiovasculaires. Pour cela, les chercheurs s’appuient sur des outils d’apprentissage automatique et d’intelligence artificielle, qui permettent de traiter de grandes quantités de données d’imagerie et de générer des outils de prédiction.
Plus précisément, le projet a débuté avec un trait connu sous le nom de tortuosité des vaisseaux rétiniens, qui caractérise la « sinuosité » des petites artères et veines alimentant les récepteurs de lumière dans l’œil. Il a été démontré que ce trait dépend fortement de la génétique et qu’il est fortement associé à des facteurs de risque cardiovasculaire, comme l’hypertension. Cette approche a ensuite été élargie à un ensemble de 17 traits vasculaires, incluant le diamètre et la densité des vaisseaux, comparés à ceux fournis par RETFound, un modèle fondation d’analyse rétinienne entraîné sur plus d’un million d’images, à l’aide des outils d’association génétique et de maladies
Le Professeur Sven Bergmann est un biologiste computationnel qui conçoit et applique de nouveaux algorithmes pour analyser de grandes quantités de données biologiques et médicales.
Faculté de biologie et médecine
GWAS, Retina, Deep learning, Foundation model, RETFound, Vasculature, CVD

